Создана искусственная жизнь из «зомби-клеток»: найден способ пересаживать синтетическую ДНК без отторжения
https://www.ixbt.com/live/science/sozdana-iskusstvennaya-zhizn-iz-zombi-kletok-nayden-sposob-peresazhivat-sinteticheskuyu-dnk-bez-ottorzheniya.htmlСоздание синтетических организмов — важная задача современной биологии. Технология конструирования геномов с нуля позволяет создавать микроорганизмы с заданными свойствами, которые могут производить редкие медицинские препараты, перерабатывать пластик или синтезировать экологически чистое топливо. Однако на пути к массовому применению этой технологии стояла проблема, связанная с естественными защитными механизмами живых клеток.
Исследователи из Института Крейга Вентера опубликовали работу, в которой описали метод обхода биологических ограничений. Они доказали, что для успешной пересадки искусственного генетического кода клетку-реципиента необходимо предварительно умертвить. Разработанный ими протокол позволяет внедрять синтетическую ДНК в биологически неживую оболочку, после чего клеточные процессы восстанавливаются, и организм начинает функционировать исключительно по новому коду. Этот подход решает проблему, которая сдерживала развитие отрасли более десяти лет.
Проблема гомологичной рекомбинации и ложных результатов
В 2010 году Институт Крейга Вентера впервые в истории успешно внедрил полностью синтетический геном в живую бактерию. Этот процесс получил название полногеномной трансплантации (Whole Genome Transplantation, или WGT). Суть метода заключалась в том, что ДНК, собранная в лаборатории, помещалась внутрь бактерии-реципиента, после чего клетка начинала считывать новую информацию и менять свои свойства.
Но вскоре ученые столкнулись с серьезным ограничением. Метод WGT безотказно работал только в пределах очень узкой группы бактерий — микоплазм (в частности, таксона Mycoides). Как только исследователи пытались применить эту технологию к другим видам микроорганизмов, эксперименты заканчивались неудачей. Причиной стал процесс, известный в биологии как гомологичная рекомбинация.
Гомологичная рекомбинация — это базовый механизм восстановления и обмена генетической информацией, присутствующий у большинства живых существ. Когда ученые внедряли гигантскую молекулу синтетической ДНК в живую бактерию других видов, клетка воспринимала ее как материал для взаимодействия.
Чтобы отслеживать успешность трансплантации, ученые всегда встраивали в искусственный геном ген устойчивости к определенному антибиотику. После проведения процедуры трансплантации все клетки помещались в среду, содержащую этот антибиотик. Предполагалось, что исходные клетки погибнут, а выживут только те, которые успешно приняли новый синтетический геном и приобрели устойчивость.
Однако из-за активности ферментов гомологичной рекомбинации живые бактерии-реципиенты не заменяли свой геном целиком. Вместо этого они просто вырезали из плавающей внутри них синтетической ДНК небольшой фрагмент, содержащий ген устойчивости к антибиотику, и встраивали его в свою собственную, оригинальную хромосому. Оставшаяся часть искусственного генома при этом разрушалась.
В результате на питательной среде с антибиотиком вырастали колонии бактерий. Ученые фиксировали положительный результат, но при детальном анализе выяснялось, что это ложное срабатывание. Выжившие колонии состояли из старых бактерий-реципиентов, которые лишь слегка модифицировали свою ДНК, а не из новых организмов, управляемых полностью искусственным кодом. Стало очевидно, что для успешной пересадки необходимо найти способ полностью деактивировать собственный геном реципиента до того, как он вступит в реакцию с новой ДНК.
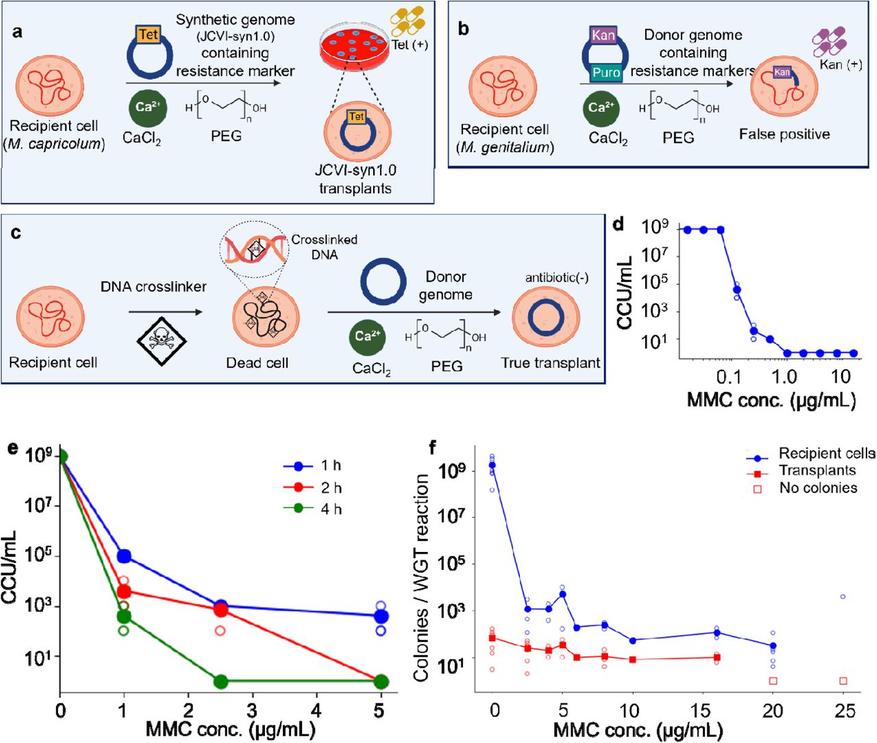
Обработка митомицином С (MMC) перед процедурой WGT инактивирует клетки-реципиенты, но сохраняет их способность принять новый геном.
(a) Схема классической процедуры полногеномной трансплантации (WGT). Донорский геном JCVI-syn1.0, содержащий ген устойчивости к тетрациклину, пересаживают в активные клетки-реципиенты M. capricolum. При помещении на питательную среду с антибиотиком сохраняются только успешные трансплантаты, принявшие новую ДНК.
(b) Механизм ложного срабатывания из-за гомологичной рекомбинации на примере бактерий M. genitalium. Вместо того чтобы принять искусственную хромосому целиком, бактерия-реципиент вырезает из донорской ДНК только нужный фрагмент (маркер устойчивости к канамицину) и встраивает его в свой родной геном. В результате на среде с антибиотиком продолжают расти старые бактерии, давая ложноположительный результат.
(c) Схема трансплантации без использования антибиотиков (новый метод). Добавление MMC химически «сшивает» собственную ДНК клеток-реципиентов M. capricolum, необратимо блокируя их жизнедеятельность. Однако те неактивные оболочки, внутрь которых попадает донорский геном, полностью восстанавливают свои функции.
(d) Определение минимальной дозы MMC, необходимой для подавления активности клеток M. capricolum. Это позволило подобрать идеальную концентрацию для экспериментов с WGT.
(e) График падения жизнеспособности клеток M. capricolum в зависимости от увеличения концентрации MMC и времени воздействия.
(f) Влияние дозы MMC на жизнеспособность клеток и эффективность самой трансплантации. При оптимальной дозировке активность старых клеток-реципиентов падает колоссально — примерно в миллион раз (≈10⁶), тогда как эффективность внедрения нового генома снижается лишь в 10 раз. При слишком высоких дозах MMC (20 и 25 мкг/мл) трансплантация становится невозможной. (На графике пустые кружки обозначают результаты отдельных экспериментов, а закрашенные — средние значения).
Автор: Zumra Peksaglam Seidel et al. Источник: www.biorxiv.org
Избирательная химическая инактивация ДНК
Самым логичным решением было отключить исходную ДНК клетки. Однако стандартные методы уничтожения бактерий, такие как радиационное облучение, сильный нагрев или воздействие агрессивных кислот, не подходили. Эти методы физически разрушают все структуры клетки: клеточную мембрану, рибосомы, белки и ферменты. Если разрушить этот аппарат, клетка потеряет способность прочитать любую ДНК, включая искусственную. Трансплантация станет невозможной.
Исследователям требовался метод, который воздействовал бы исключительно на генетический материал, оставляя все остальные клеточные компоненты нетронутыми. Они обратились к химическим веществам, способным формировать необратимые связи внутри молекулы ДНК.
Основным инструментом в исследовании стал митомицин С (MMC) — химическое соединение, относящееся к классу алкилирующих агентов. При попадании в клетку митомицин С избирательно находит гуаниновые основания в ДНК и образует между ними прочные ковалентные связи. ДНК представляет собой двойную спираль, нити которой должны расплетаться в процессе деления клетки или при считывании информации. Митомицин С скрепляет эти две нити вместе. Из-за таких химических сшивок механизмы репликации останавливаются. Бактерия необратимо теряет способность копировать свой геном и делиться. С биологической точки зрения она становится мертвой (Моё примечание: некорректное умозаключение, что становится мёртвой.).
Ученые провели серию экспериментов на бактериях Mycoplasma capricolum, чтобы найти идеальную дозировку. Выяснилось, что при концентрации митомицина С в 2,5 микрограмма на миллилитр и времени воздействия в два часа достигается нужный эффект. Собственный геном бактерии полностью выводится из строя, но рибосомы, транскрипционные ферменты и клеточная мембрана сохраняют свою функциональность. Клетка мертва для деления (Моё примечание: вот именно – она «мертва» только для деления.), но ее механизмы синтеза белка готовы к работе.
Для подтверждения того, что успех обусловлен именно принципом связывания ДНК, а не уникальными свойствами конкретного химиката, ученые протестировали другое вещество — псорален. Псорален проникает между парами оснований ДНК, но активируется и создает сшивки только под воздействием ультрафиолетового излучения (UVA). Эксперимент показал аналогичные результаты, доказав, что контролируемая инактивация ДНК является универсальным подходом.
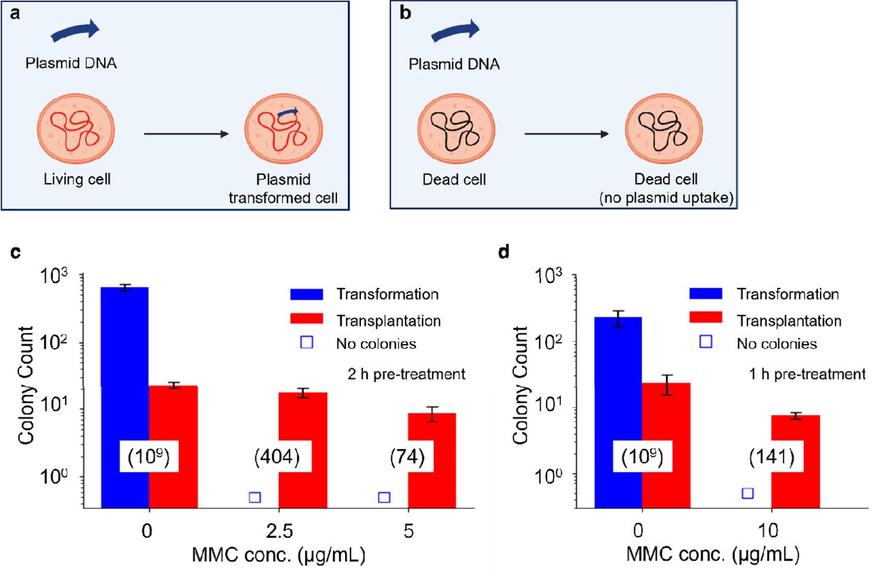
Обработка MMC делает возможной процедуру WGT в инактивированных клетках-реципиентах.
На схемах показано сравнение трансформации плазмиды (кольцевой молекулы ДНК) в (a) активных и (b) лишенных жизнеспособности клетках-реципиентах. Бактерии с химически заблокированным геномом оказались неспособны к трансформации плазмиды. Эффективность этого процесса сравнили с полногеномной трансплантацией (WGT) после воздействия MMC.
Результаты экспериментов с клетками, обработанными препаратом в дозе 2,5 или 5 мкг/мл в течение двух часов (c), а также 10 мкг/мл в течение одного часа (d), доказывают, что пересадка генома успешно проходит даже в полностью неактивных клеточных оболочках. Цифры в скобках указывают на количество оставшихся жизнеспособных клеток для каждого из условий.
Автор: Zumra Peksaglam Seidel et al. Источник: www.biorxiv.org
Процесс трансплантации без использования антибиотиков
Получив раствор с неживыми бактериями (Моё примечание: Не «с неживыми» бактериями, а с бактериями с «отключенной» ДНК.) Mycoplasma capricolum, исследователи приступили к этапу внедрения синтетического генома. В качестве донорского материала использовалась искусственная хромосома JCVI-syn1.0. С помощью химических реагентов (кальция хлорида и полиэтиленгликоля) клеточные мембраны бактерий делали проницаемыми, чтобы массивная молекула ДНК могла проникнуть внутрь.
Поскольку собственный геном реципиентов был разрушен митомицином С, процесс гомологичной рекомбинации физически не мог запуститься. Оболочка приняла донорскую ДНК. Оставшиеся внутри клетки активные транскрипционные ферменты начали взаимодействовать с новым генетическим кодом. Они стали синтезировать новые матричные РНК, которые затем передавались на рибосомы для производства белков, закодированных в синтетической хромосоме. Клеточная активность полностью восстановилась.
Самым важным достижением этого протокола стала возможность полного отказа от антибиотиков при отборе успешных трансплантатов. В классическом методе на чашках Петри без антибиотика вырастал бы сплошной слой старых бактерий, среди которых невозможно было бы найти несколько клеток с новым геномом. В новом эксперименте исследователи высеивали результаты на обычную питательную среду без добавления токсичных веществ.
Так как все исходные клетки были предварительно умерщвлены (Моё примечание: не были они умерщвлены.) митомицином С, они не могли делиться и образовывать колонии. Единственными клетками, которые демонстрировали рост и деление на питательной среде, оказались те бактерии, которые успешно приняли внутрь себя синтетический геном JCVI-syn1.0.
Для визуального подтверждения в синтетическую хромосому был заранее внедрен ген lacZ. Бактерии, обладающие этим геном, при взаимодействии со специальным веществом в питательной среде окрашиваются в синий цвет. Все выросшие колонии оказались синими. Дополнительный лабораторный анализ с помощью мультиплексной полимеразной цепной реакции (ПЦР), который проверил одиннадцать специфических участков ДНК, окончательно подтвердил: выросшие бактерии обладают исключительно синтетическим геномом. Никаких следов старой ДНК Mycoplasma capricolum в активном виде обнаружено не было.
Исследователи подсчитали эффективность нового метода. При использовании живых реципиентов успешная пересадка происходила примерно в одном случае на 150 миллионов клеток. При использовании неживых клеток общее количество выживших микроорганизмов резко упало, но относительная эффективность внедрения новой ДНК возросла. Один успешный трансплантат приходился всего на 288 жизнеспособных клеток. Это означает увеличение эффективности процедуры более чем в 500 000 раз.
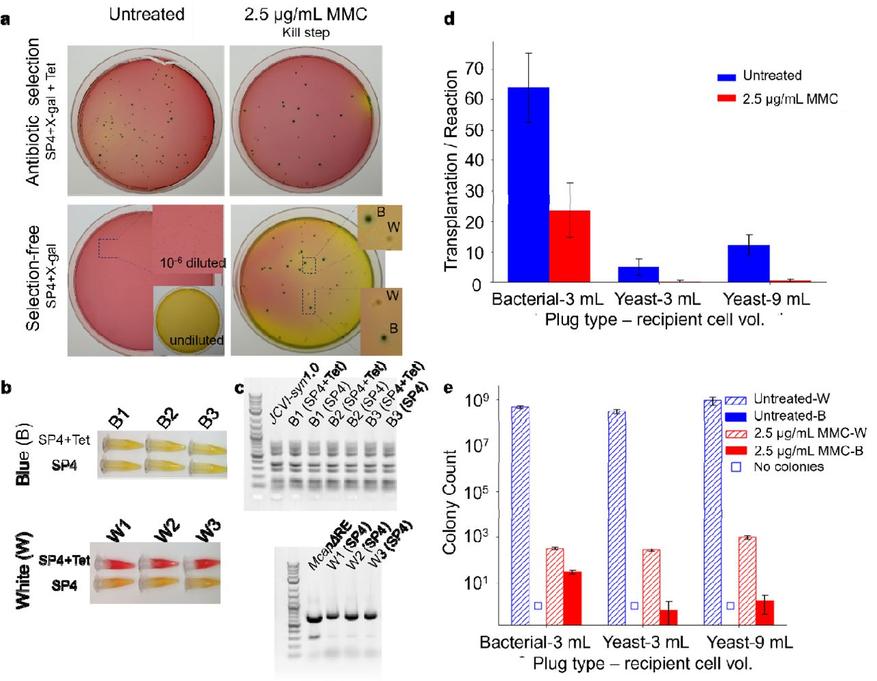
Обработка MMC в процессе WGT позволяет отказаться от использования антибиотиков для отбора трансплантатов. Ученые сравнили эффективность метода WGT с использованием антибиотиков и без них, проводя процедуру как с предварительной обработкой MMC, так и без нее. (a) Фотографии чашек Петри с питательной средой. Белые колонии — это исходные клетки M. capricolum, синие — успешные трансплантаты JCVI-syn1.0. Геном JCVI-syn1.0 содержит маркер устойчивости к тетрациклину, поэтому он способен расти на среде как с антибиотиком, так и без него. Исходные же клетки M. capricolum растут только на среде без антибиотика. (b) Культивирование образцов в пробирках со средой SP4. Рост бактерий сопровождается повышением кислотности среды, из-за чего индикатор (феноловый красный) меняет цвет с красного на желтый. (c) Генетическое подтверждение состава колоний с помощью мультиплексной ПЦР. Тесты (b) и (c) подтвердили, что белые колонии состоят из исходных клеток, а синие являются трансплантатами JCVI-syn1.0. (d) Измерение эффективности трансплантации для обычных и инактивированных (обработанных MMC) клеток-реципиентов при использовании донорских геномов, полученных из бактерий или дрожжей. (e) Сравнение количества колоний на средах без антибиотиков. Без предварительной блокировки исходного генома обычные клетки-реципиенты растут слишком плотно, образуя сплошной «газон». Это делает невозможным выделение отдельных трансплантатов без применения антибиотиков. (На графиках (d) и (e) представлены средние арифметические значения, а планки погрешностей отражают стандартное отклонение по результатам трех независимых биологических опытов).
Автор: Zumra Peksaglam Seidel et al. Источник: www.biorxiv.org
Значение для науки и биотехнологий
Этот эксперимент наглядно демонстрирует, что граница между живой и неживой клеткой определяется не столько физической целостностью организма, сколько способностью генома к репликации (Моё примечание: зрелый эритроцит тоже неживой, что ли? У него ДНК вообще нет.). Процесс загрузки жизни не требует полностью функционального реципиента. Минимально необходимым условием является наличие неповрежденного транскрипционного и трансляционного аппарата.
На практике этот прорыв снимает главное техническое препятствие для расширения методов синтетической биологии. Исключение проблемы гомологичной рекомбинации означает, что ученым больше не нужно ограничиваться только микоплазмами. Технология открывает путь к стандартизации процесса. В будущем исследователи смогут подготавливать универсальные, лишенные собственной генетической информации клеточные оболочки различных видов бактерий.
Эти подготовленные пустые клетки будут служить базовыми платформами для внедрения любых спроектированных на компьютере генетических последовательностей. Такая технология многократно ускорит создание специализированных микроорганизмов для нужд медицины (например, для синтеза сложных белковых соединений и новых антибиотиков), биотехнологической промышленности и защиты окружающей среды, позволяя конструировать живые системы с такой же точностью, с какой инженеры собирают сложные технические устройства.
Источник: biorxiv
P.S. Проводить границу между живым и неживым по способности к репликации (например, «отключив/заблокировав» ДНК) некорректно.
Эритроциты в зрелом состоянии ДНК вообще не имеют. У человека они живут в таком виде примерно 120 суток.
Эритроциты
https://ru.wikipedia.org/wiki/%D0%AD%D1%80%D0%B8%D1%82%D1%80%D0%BE%D1%86%D0%B8%D1%82%D1%8BЗрелый эритроцит, с диаметром 7—8 мкм, не имеющий ядра и ДНК (в центре — просветление), цитоплазма — розово-красная.
...
Продолжительность жизни эритроцита человека около — 120 суток
 Интересные новости и факт...
от ArefievPV
Интересные новости и факт...
от ArefievPV  Интересные новости и факт...
от ArefievPV
Интересные новости и факт...
от ArefievPV  Интересные новости и факт...
от ArefievPV
Интересные новости и факт...
от ArefievPV  Понимание и взаимопониман...
от ArefievPV
Понимание и взаимопониман...
от ArefievPV  Интересные новости и факт...
от ArefievPV
Интересные новости и факт...
от ArefievPV 



